PDF-Version
Faktenwissen
Der erstaunliche Hebelmechanismus des Wiesensalbeis
Evolution "nichtreduzierbar komplexer Systeme"
REGINE CLAßEN-BOCKHOFF & MARTIN NEUKAMM
Erschienen in: Biologie in unserer Zeit 2/2026 (56), 166-174
Fast 20 Prozent der deutschen Bevölkerung zweifeln an der Evolutionstheorie [1], darunter 16 Prozent der Lehramtsstudierenden und 7 Prozent der angehenden Biologielehrer und -lehrerinnen [2]. Die Zurückweisung der Evolutionstheorie erfolgt im Wesentlichen aufgrund religiöser Überzeugungen [3], wird aber mit scheinbar wissenschaftlichen Argumenten begründet. Diese Art von Evolutionskritik kursiert im Internet, an Schulen und Universitäten – wie lässt sie sich argumentativ entkräften?

Die Idee, aus der zweckmäßigen Komplexität der Natur auf einen intelligenten Zwecksetzer (Schöpfergott, Designer) zu schließen, hat eine lange Tradition. Bereits der englische Theologe William PALEY verglich in seinem Werk Natural Theology (1802) [4] die Welt mit einer Taschenuhr: Wie die präzis aufeinander abgestimmten Teile einer Uhr auf einen Uhrmacher hindeuten, so weise auch die Ordnung der Welt auf einen intelligenten Designer hin. Im Zentrum des Analogiearguments stehen biologische Strukturen. PALEY wählt als einführendes Beispiel den Vergleich zwischen Auge und Teleskop: Beide Instrumente erfüllten einen konkreten Zweck und seien nach den Gesetzen der Optik konstruiert. In der Komplexität, Feinheit und Raffinesse ihrer Funktionsmechanismen offenbare sich daher ein planender Geist.
Allerdings zeigte bereits 25 Jahre vor PALEY der schottische Philosoph David HUME in seinem Buch Dialogues Concerning Natural Religion [5], dass solche Analogieargumente philosophisch schwach sind. Der Schluss von einer Uhr auf einen Uhrmacher ist stark, weil er sich aus der Erfahrung speist. Schon einfachste Relikte wie Tonscherben identifizieren wir aufgrund von Erfahrungswissen als Artefakte. Ein solches Wissen existiert bei Lebewesen und dem Universum als Ganzes nicht, im Gegenteil: Da sich natürliche Systeme in wesentlichen Eigenschaften – insbesondere in ihrer Fähigkeit zur Selbstorganisation – von Artefakten unterscheiden, ist der Schluss auf einen Designer kein empirisches Argument, sondern setzt stillschweigend theologische Zusatzannahmen voraus.
HUME argumentiert, dass – soweit wir a priori wissen – auch der Materie eine Quelle der Ordnung innewohnen könne, ohne dass sie diese von außen erworben hat. Heute würden wir von der Fähigkeit materieller Objekte zur Strukturbildung bzw. Selbstorganisation sprechen.
Freilich konnte HUME noch keine wissenschaftliche Erklärung für die natürliche Entstehung der Arten und ihrer zweckmäßigen Organe liefern. Erst Charles DARWIN formulierte in On the Origin of Species (1859) [6] mit seiner Theorie der natürlichen Auslese (Selektionstheorie) einen überzeugenden Ansatz, der die Entwicklung komplexer Strukturen ohne planenden Eingriff verständlich macht – auch wenn er die Mechanismen der Variation und Vererbung noch nicht im Einzelnen kannte. Richard DAWKINS beschreibt in The Blind Watchmaker (1986) [7] anschaulich, wie im Wechselspiel aus zufälligen Mutationen und anschließender Selektion auch komplexe Organe wie das Auge der Wirbeltiere evolvieren konnten.
Vom "Design"-Argument zum Argument der nichtreduzierbaren Komplexität
Solche Beispiele haben allerdings oft eine entscheidende Schwäche: Selektion kann nur wirken, wenn bereits eine funktionelle Struktur vorhanden ist, deren Leistung sich schrittweise verbessern lässt. "Halbe" Augen – wie etwa die Pigmentbecheraugen der Lanzettfischchen – ermöglichen zwar kein scharfes Sehen wie das Wirbeltierauge, bieten aber eine rudimentäre Form des Richtungssehens, die sich graduell optimieren lässt. Ohne die in den Fotorezeptoren ablaufende Prozessfolge der visuellen Signaltransduktion allerdings ist kein Selektionsgradient gegeben, der kontinuierlich eine Verbesserung der Sehfunktion bewirken könnte. Fehlt nur ein Glied in der molekularen Signalübertragungskette, bricht der Sehvorgang ab.
An dieser Stelle schalten sich die Evolutionskritiker ein. Diese fassen gern biologische Systeme ins Auge, deren Komponenten so miteinander wechselwirken, dass sie gemeinsam eine neue biologische Funktion ausüben. Lässt sich die Komplexität des Systems an keiner Stelle vereinfachen, ohne dass es seine Funktion einbüßt, sprechen sie von "nichtreduzierbar komplexen Systemen".
BEHE [8] argumentiert, es sei nicht vorstellbar, dass solche Systeme schrittweise über einen hinreichend wahrscheinlichen Weg aus einfachen Vorläufersystemen ohne diese Funktion evolvierten. Da potenziell vorteilhafte Mutationen ihren Besitzern so lange keinen Selektionsvorteil bescherten, wie nicht alle notwendigen Mutationen aufgetreten seien, die es für die spezifische Funktion brauche, würden potenzielle Vorstufen wieder ausgemerzt. Denkbar sei daher nur eine konzertierte Entstehung, wobei alle Teile des Systems in einem Schritt entstanden und passend aufeinander abgestimmt worden seien. Für einen "blinden" Naturprozess wie Evolution sei ein solcher Sprung beliebig unwahrscheinlich. Folglich, so die Argumentation, müssten die betreffenden Systeme von einem "intelligenten Schöpfer" (z.B. einer Gottheit) "ausgedacht" worden sein.
Der Versuch, aus der Zweckhaftigkeit und Komplexität von Naturgegenständen auf einen göttlichen Planer (Designer), Zwecksetzer oder Schöpfer zu schließen, entspricht der Strategie des Intelligent Designs [9]. Dabei handelt es sich um eine Spielart des Kreationismus, die zugesteht, dass sich das Leben in Jahrmilliarden entfaltete, eine Makroevolution jedoch ablehnt und stattdessen schöpferische Eingriffe (Design) postuliert.
Gern zitierte Beispiele für "nichtreduzierbare" Komplexität sind Blüten mit besonderen Bestäubungsmechanismen wie zum Beispiel der Hebel- oder Schlagbaummechanismus des Wiesensalbeis (Abbildung 1).

a) Blütenstand mit Lippenblüten. Der Pfeil weist auf die unter der Oberlippe verborgenen Pollensäcke hin. b) Die Honigbiene hat den Hebelmechanismus ausgelöst und wird auf dem Rücken mit Pollen belegt. c) Längsschnitt durch eine Blüte mit Barriere im Blüteneingang, Nektarangebot am Grund der Kronröhre, Oberlippe, Unterlippe und Staminalhebel. d) Pollenübertragung von einer jungen Blüte auf den Rücken des Bestäubertieres. e) Abstreifen des Pollens vom Bestäuberrücken auf die Narbe einer älteren Blüte. Ba = Barriere im Blüteneingang, Ne = Nektarquelle, Ol = Oberlippe, Sh = Staminalhebel, Ul = Unterlippe. Abb. aus [13], [14], [15].
Nach JUNKER und WIDENMEYER [10, S. 209] zeigt das System zwei Design-Indizien. Zum einen sei es "nichtreduzierbar komplex": "Blütenform, seitliche Verwachsung der Staubfäden, Gelenk, Platte und Timing" müssen komplett vorhanden und aufeinander abgestimmt sein; fehle ein Bauelement, habe das den totalen Funktionsausfall zur Folge. Das Schlagbaum-System könne erst ausgelesen werden, wenn es als Ganzes vorhanden sei, ein schrittweiser Aufbau über ungerichtete Mutationen und in jeder Generation wirksame Auslese sei nicht denkbar. Zum anderen erscheine das Schlagbaum-System als "spielerische Komplexität", denn es fehle einigen Salbeiarten, die nicht weniger überlebensfähig seien. Aus funktionaler Sicht sei die Schlagbaumkonstruktion daher unnötig und ein fantasievolles Extra, ein Design-Indiz.
WIDENMEYER und JUNKER [11] legen die Struktur des "Design-Arguments in der Biologie" in allgemeiner Form dar; warum ihre Argumentation sowohl wissenschaftlich als auch philosophisch nicht tragfähig ist, erläutert Neukamm [12].
Bezogen auf das Beispiel des Wiesensalbeis liegt ein zentrales Problem in der Blickrichtung: Hat man den fertig funktionierenden Hebelmechanismus vor Augen, steht man tatsächlich vor einem erstaunlichen System, dessen Evolution schwer vorstellbar ist. Bezieht man aber Entwicklung, Vielfalt und Stammesgeschichte der Gattung Salvia mit in die Betrachtung ein, lässt sich sein Zustandekommen durchaus rekonstruieren.
Morphologie und Funktionsweise des Hebelmechanismus beim Wiesensalbei
Der allgemein bekannte Hebel- oder Schlagbaummechanismus des Wiesensalbeis wird durch Hummeln und Bienen ausgelöst, die sich auf die Unterlippe der Blüte setzen, um an den Nektar der Blüte zu gelangen (Abbildung 1c). Dabei stoßen sie gegen eine Barriere im Blüteneingang, schieben diese zurück und werden durch die sich absenkenden Pollensäcke mit Pollen beladen (Abbildungen 1b, d). Beim Anflug auf eine andere, etwas ältere Blüte wird der Pollen auf die Narbe abgegeben (Abbildung 1e): Die Bestäubung ist erfolgt.
Wie kommt es zu dieser Form der Pollenübertragung? Der Wiesensalbei besitzt eine Lippenblüte, die aus Ober- und Unterlippe besteht (Abbildungen 1c, 2d). Die Oberlippe ist helmförmig gestaltet und verbirgt den Pollen (Abbildung 1a, Pfeil), während die Unterlippe den Blütenbesuchern als Sitzplatz dient. Ober- und Unterlippe gehen zum Fruchtknoten hin in die Kronröhre über, an deren Grund Nektar produziert wird (Abbildung 1c). Die Blüte weist zwei Staubträger (Stamina) auf, die mehr oder weniger weit mit der Kronröhre verbunden sind (Abbildung 2c). Die Staubträger bestehen aus je einem Filament (Staubfaden) und einer Anthere (Staubbeutel). Aufgrund einer Dünnstelle zwischen Filament und Konnektiv (Gelenk) ist die Anthere gegenüber dem Filament beweglich (versatil). Sie besteht aus zwei Hälften, den Theken, die jeweils zwei Pollensäcke tragen (Abbildung 2a).
Zwischen den Theken liegt das Konnektiv, ein Gewebeband, in dem das Leitbündel der Anthere verläuft. Es ist stark verbreitert und formt zwei Konnektivarme, die wie Hebelarme um das Gelenk schwingen können (Abbildung 2b). Filament- und Konnektivauswüchse stabilisieren die Bewegung (Abbildung 2c) [13]. Der obere Konnektivarm trägt eine fertile Theke mit zwei Pollensäcken, der untere ist steril und zu einer schaufelförmigen Druckplatte umgebildet. Er versperrt den Blüteneingang und damit den Zugang zum Nektar. Stößt ein Blütenbesucher gegen die Druckplatte, löst er den Hebelmechanismus aus: Die Pollensäcke senken sich auf den Kopf oder Rücken ab und schwingen wieder zurück, sobald das Insekt die Blüte verlassen hat.
Entwicklung des staminalen Hebelmechanismus in der Blüte
Der Wiesensalbei (Salvia pratensis) gehört zur Gattung Salvia, mit etwa 1.000 Arten die artenreichste Gruppe der Lippenblütler (Lamiaceae). Innerhalb der Familie steht die Gattung in der artenreichen Tribus Mentheae (Unterfamilie Nepetoideae). Die meisten Lippenblütler weisen die namensgebende Lippenblüte auf. Sie besitzen vier mit der Kronröhre verbundene Staubträger und bieten Nektar am Grund der Blütenröhre an.
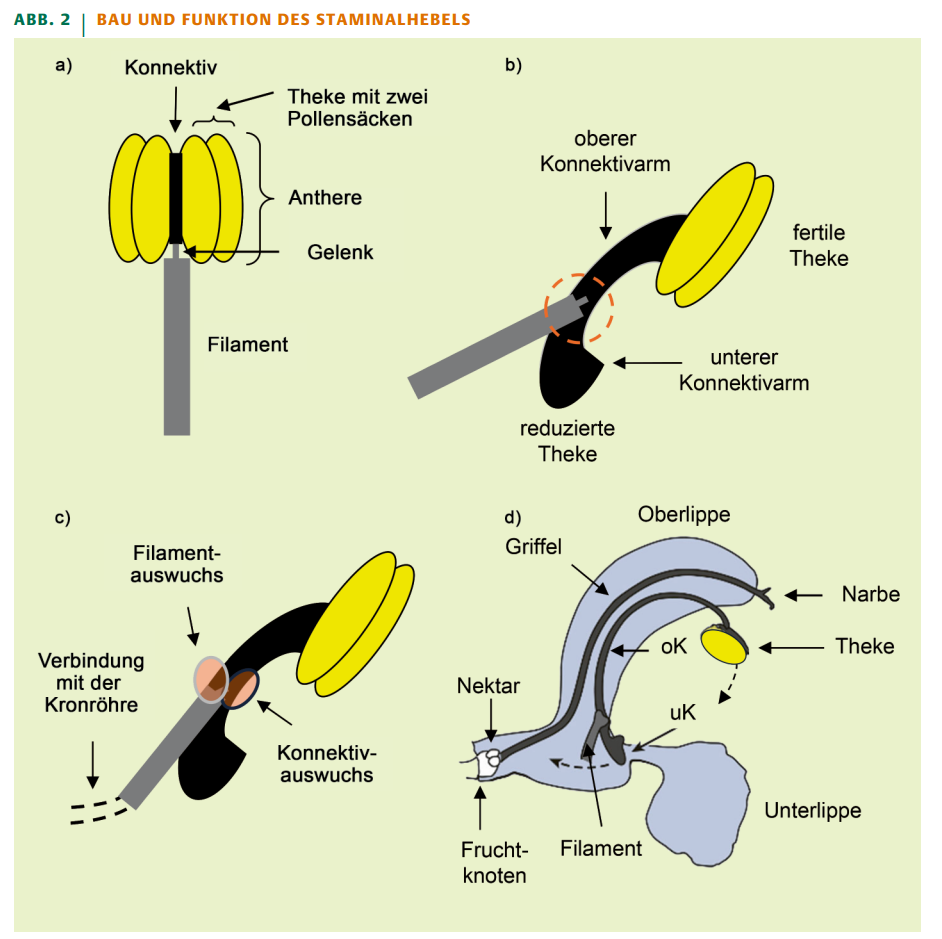
a) Allgemeiner Bau eines Staubträgers (Stamen) bei Blütenpflanzen mit Anthere, Filament (im Beispiel mit Gelenk) und Konnektiv. b, c), Stamenbau beim Wiesensalbei. b) Das Konnektiv ist verbreitert und bildet einen oberen fertilen Konnektivarm (mit Theke und zwei Pollensäcken) und einen unteren sterilen Konnektivarm, der eine schaufelförmige Barriere im Blüteneingang bildet. Die beiden Konnektivarme sind über das Gelenk (Kreis) beweglich. c) Die Präzision der Hebelbewegung wird im Bereich des Gelenks durch Auswüchse des Filaments und Konnektivs erhöht. d) Schematischer Längsschnitt durch eine Blüte. Die gestrichelten Linien geben die Hebelbewegung wieder. Abb. aus [14],[15], c: die Autoren.
Innerhalb der Familie wurde die Anzahl der Stamina mehrfach parallel von vier auf zwei reduziert, allein fünfmal innerhalb der Mentheae [16], darunter auch in der Gattung Salvia. Die beiden charakteristischen Merkmale des Wiesensalbeis, die Konnektivstreckung und die bewegliche Anthere, fehlen einigen Salbeiarten, treten aber innerhalb der Lippenblütler bei Vertretern der australischen Prostantheroideae-Westringieae auf [17]. Bewegliche Antheren sind ein weit verbreitetes Blütenmerkmal, das auch in radiären Blüten und entfernt stehenden Verwandtschaftsgruppen vorkommt. Man sieht, dass die Komponenten des Hebelmechanismus kein Alleinstellungsmerkmal des Wiesensalbeis sind.
Die Blüte der meisten Salbeiarten wird zunächst radiärsymmetrisch angelegt und erst im Zuge ihrer weiteren Entwicklung monosymmetrisch (zygomorph) überprägt. Von den vier Staminalanlagen kommen nur zwei zur vollen Entwicklung, während die beiden anderen im Zuge der Symmetrieveränderung gehemmt bleiben (Abbildungen 3a, b). Die beiden Stamina sind seitlich an der Krone angeheftet, aus der die Antheren frei werden. Der Ort dieser Trennung ist variabel und bestimmt die Lage des Filaments. Alle diese Verhältnisse gehören zum phylogenetischen Erbe der Lippenblütler.
Jeder der beiden Staubträger bildet einen Staubbeutel mit ursprünglich zwei Thekenanlagen (Abbildung 3c). Die später unter der Oberlippe liegende Theke entwickelt sich sehr schnell und wird deutlich länger als die untere Anlage, die bei vielen Arten gehemmt bleibt (Abbildung 3c). Bereits in der Knospe verbreitert sich das Konnektiv und trennt die beiden Thekenanlagen voneinander. Dabei dreht der stark wachsende obere Konnektivast die große Theke um 90°, so dass diese in der Längsachse der Blütenknospe zu liegen kommt (Abbildungen 3d, h). Dann erst streckt sich das Filament und bildet das Gelenk mit seinen Auswüchsen, um das die Konnektivarme beweglich sind (Abbildung 3e).
Die Blütenentwicklung zeigt, dass die Entstehung des Hebelmechanismus weniger spektakulär ist als allgemein angenommen: Lippenblüte, seitliche Fixierung der Stamina, Reduktion der Stamenanzahl und bewegliche Antheren sind in der Familie weit verbreitete Merkmale. Der Hebelmechanismus entsteht erst, wenn Filament-, Konnektiv- und Blütenproportionen spezifisch zueinander passen. Wie kommt es zu dieser funktionalen Kooperation?
Alle Blütenstrukturen entstehen aus Anlagen, die zunächst nur wenige Zellen umfassen. Mutative Änderungen, die in der Blütenentwicklung zu minimaler Lageverschiebung, Hemmung oder Förderung führen, haben große Auswirkungen in der fertigen Blüte. Einzelne Entwicklungsschritte können dabei im Vergleich zu einem Vorfahren schneller oder langsamer ablaufen, früher oder später einsetzen, verkürzt oder verlängert werden, wegfallen oder neu hinzukommen. Viele Formen werden ausprobiert, eliminiert oder als vorteilhafte Neubildungen beibehalten. Dafür stehen Millionen Jahre Evolutionszeit zur Verfügung.
Betrachtet man heute existierende Blüten, erscheinen einige komplexe Strukturen in Form und Funktion "aufeinander abgestimmt" zu sein. Sie sind aber nicht das Ergebnis einer "zielgerichteten" oder "geplanten" Entstehung, sondern beruhen auf natürlicher Variation und Selektion in einem sehr langen Zeitraum. Die funktionelle Passung ist das Ergebnis von Co-Variation und Co-Adaptation ursprünglich unabhängiger Blütenelemente, die als Synorganisation bezeichnet wird. Synorganisation gilt als einer der wichtigsten Evolutionsprozesse [18].
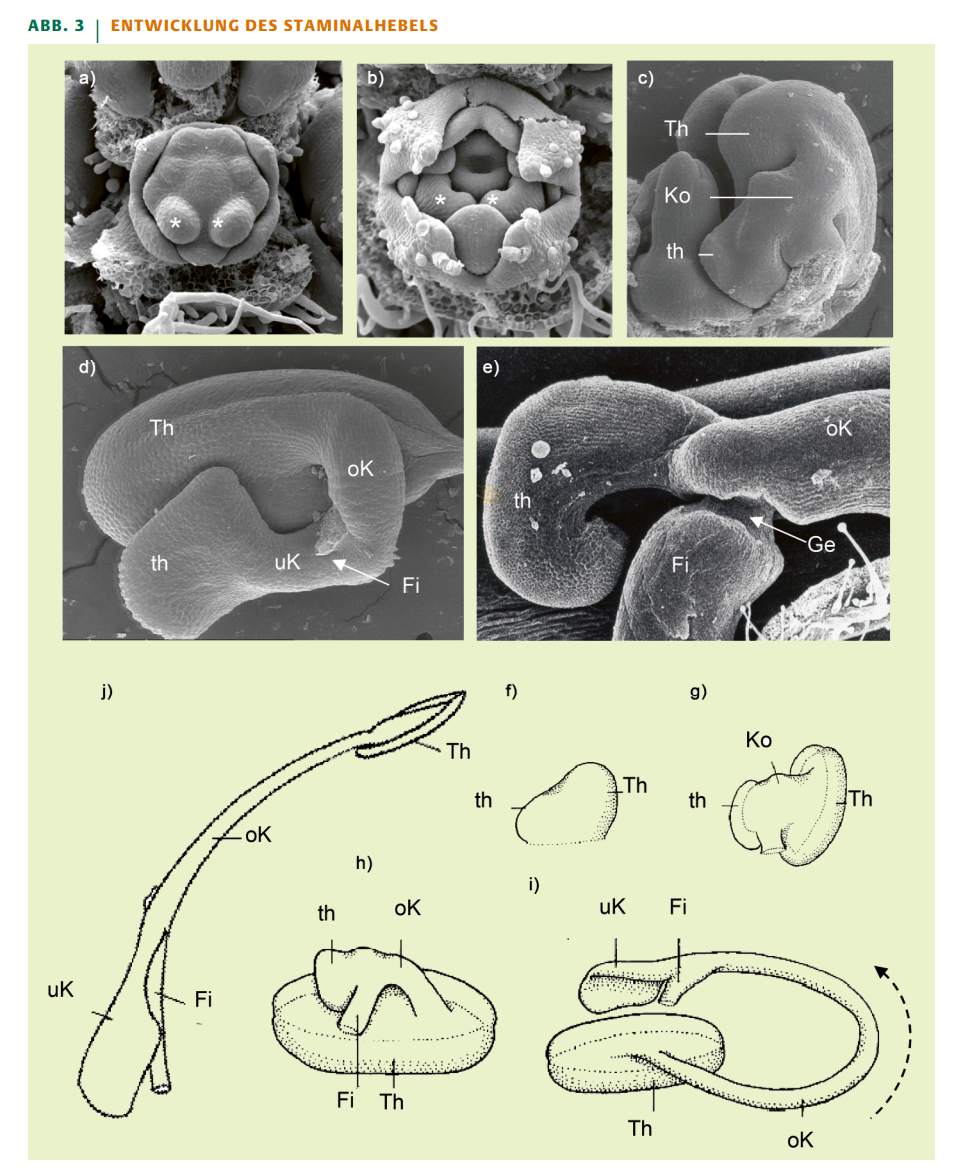
a, b) Salvia verticillata: a) Junge, noch fast radiäre Blütenanlage; die beiden geförderten Staminalanlagen sind mit einem Sternchen markiert. b) Etwas ältere, bereits zygomorph überprägte Blütenanlage. c, d) S. uliginosa: c) Seitenansicht auf eine Staminalanlage mit geförderter Theke und gehemmt bleibender Theke. d) Der obere Konnektivarm verlagert die geförderte Theke, so dass sie längs in der Blütenknospe liegt. e) S. glutinosa: Das unverdickte Ende des Filaments bildet das Gelenk, das von Auswüchsen des Konnektivs und Filaments überwallt wird. f–j) S. pratensis: Schematische Darstellung der Stamenentwicklung. Der gestrichelte Pfeil in i) gibt die Aufrichtung der Anthere bei der Blütenöffnung wieder. Fi = Filament, Ge = Gelenk, Ko = Konnektiv, oK = oberer Konnektivarm, Th = geförderte Theke, th = gehemmt bleibende Theke, uK = unterer Konnektivarm. Abb. a, b: N. Daichendt und R. Claßen-Bockhoff, Mainz. c–e) aus [13], f–j aus [19], verändert.
Die strukturelle Vielfalt des Wiesensalbeis und seiner Verwandten
Die meisten, aber nicht alle Arten der Gattung Salvia (Abbildung 4) weisen einen funktionierenden Hebelmechanismus auf. Die Vielgestaltigkeit der Stamina lässt sich in fünf Gruppen einteilen. Anhand der unterschiedlichen Merkmalskombinationen können die evolutive Entstehung und sekundäre Reduktion des Hebelbaus rekonstruiert werden [20], [21]:
Die Gruppe I (Abbildung 4: grau) umfasst Arten ohne Hebelmechanismus. In den artenarmen Untergattungen Perovskia, Meriandra und Dorystaechas sowie bei S. majdae (Untergattung Zhumeria) weisen die Antheren je zwei fertilen Theken (dithecisch) auf, die nur durch eine geringe Konnektivstreckung voneinander separiert sind (Abbildung 4 Ia, b). In der ebenfalls artenarmen Gruppe Echinosphace (Untergattung Audibertia) treten dagegen dithecische Antheren mit deutlich verbreiterten Konnektiven auf (Abbildung 4 Ic). Bei allen diesen Arten wird der Pollen vom Blütenbesucher abgestreift.
Die Gruppen II-IV weisen typische Hebelmechanismen mit beweglichen Antheren und Konnektivstreckung auf. Die Verwandtschaftsverhältnisse legen nahe, dass sie mehrfach unabhängig voneinander entstanden sind. Vertreter der Gruppe II (blau) mit dithecisch-gekrümmten Antheren kommen in allen Untergattungen mit Hebelmechanismus vor und stellen entwicklungsmorphologisch die Ausgangsform für alle weiteren Abwandlungen dar [13].
Gruppe III (grün) umfasst gekrümmte Antheren mit nur einer fertilen Theke (monothecisch), die in zwei Ausprägungsformen vorliegen. Altweltlich verbreitete Arten weisen einen sterilen, unteren Konnektivarm auf, der in vielfältiger Weise abgewandelt ist (Abbildung 4 IIIa, b). Die gestaltliche Variation beruht auf Form- und Größenveränderungen und geht oft mit Auswüchsen und Schwielen einher. Diese Antherenform ist häufig und tritt in vier Untergattungen parallel auf. Bei einigen Arten der amerikanischen Untergattung Calosphace liegt dagegen ein gekrümmtes Konnektiv mit einem rückenwärtigen Auswuchs vor, der der Anthere eine gerade Form verleiht (Abbildung 4 IIIc).
Gerade Antheren (Gruppe IV, rot) sind charakteristisch für die übrigen Arten der Untergattung Calospace. Sie sind monothecisch (Gruppe IVa) und weisen oft ventrale Auswüchse ("Zähne") auf (Gruppe IVb) [22]. Bei zahlreichen Arten ist die Blüte so eng, sodass der Hebel nicht mehr ausgelöst werden kann: Der Pollentransfer via Hebelmechanismus geht verloren. Pollensäcke und Narbe ragen aus der Blüte heraus. Dieser Umbau der Blüte geht mit einem Bestäuberwechsel von Bienen zu Kolibris einher. Beim Anflug des Vogels wird der mitgebrachte Fremdpollen auf der Narbe abgestreift und anschließend der Eigenpollen auf dem Tier abgelegt [23].
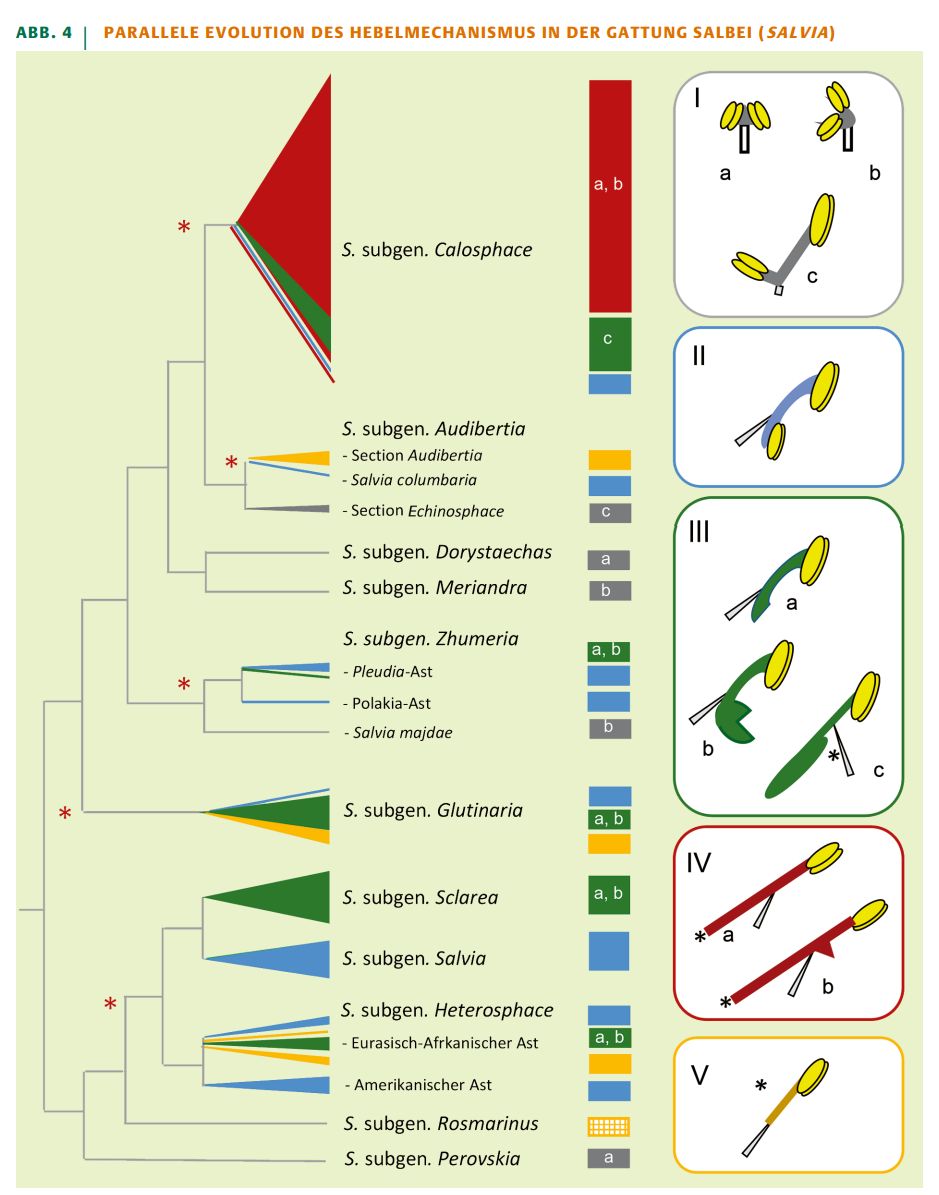
Auf der linken Seite ist der Stammbaum der Gattung dargestellt, der 11 Untergattungen (subgen.) mit teilweise mehreren Untergruppen (Äste) umfasst. Die Farben verweisen auf die fünf farbig umrahmten Stamentypen (I–V, s. Text) und ihre Unterformen (a–c), die rechts dargestellt sind. In der Mitte erfolgt die Zuordnung der Stammbaumäste mit den darin auftretenden Stamenformen. Die Balken entsprechen den Ästen, die Farben und Kleinbuchstaben beziehen sich auf die Stamenformen. Es wird deutlich, dass der Hebelmechanismus mindestens fünfmal parallel entstanden (rote Sternchen) und dreimal reduziert worden ist (Typ V). Der Stamentyp von Salvia subgen. rosmarinus ähnelt Typ V, ist aber vermutlich nicht durch Reduktion eines Hebels entstanden. Stammbaum nach [26] und [27], Stamentypen nach [20].
Das Beispiel zeigt, dass Krone und Staminalapparat unabhängig voneinander variieren, wodurch die Synorganisation der Teile verloren geht. Es zeigt weiterhin, dass der Funktionsverlust des Hebelmechanismus durch eine andere Art der Pollenübertragung kompensiert werden kann: Die Blüten sind auch ohne Hebelmechanismus erfolgreich.
In der Gruppe V (orange Umrahmung) fehlt der Hebelmechanismus wie in Gruppe I. Allerdings bleibt hier der untere Konnektivarm unentwickelt und steht nicht als Hebelarm zur Verfügung. Während der Blütenentwicklung setzt der Hemmprozess der unteren Theke früher als bei den anderen Arten ein und unterdrückt das Wachstum des unteren Konnektiv-Abschnitts. Stamina der Gruppe V treten in vier Untergattungen auf (Abbildung 4) und sind mit verschiedenen Bestäubungsprozessen kombiniert [24],[25].
Die Evolution der Salbeiblüte und das Argument der nichtreduzierbaren Komplexität
Angesichts der enormen strukturellen und funktionellen Diversität der Salbeiblüte ist das Argument der "nichtreduzierbaren Komplexität" nicht haltbar. Zwar bilden beim Wiesensalbei verschiedene Blütenorgane gemeinsam einen funktionierenden Hebelmechanismus, der "nicht reduzierbar komplex" erscheint. Daraus folgen aber weder dessen Nicht-Evolvierbarkeit noch ein Argument für eine planmäßige Entstehung – im Gegenteil: Bezieht man die mehr als 1.000 Arten der Gattung Salvia in die Betrachtung ein, zeigt sich eine große Variationsbreite an Blütenformen und Bestäubungsmechanismen.
Alle evolutiven Einzelereignisse wie Reduktion von vier auf zwei Staubträger, Konnektivverbreiterung, Gelenkbildung, Versperrung des Blüteneingangs oder sekundäre Versteifung und Reduktion des Hebelapparates treten einzeln (isoliert voneinander) oder in unterschiedlichen Kombinationen auf. JUNKER und WIDENMEYER [10] liegen also falsch mit der Annahme, der Hebelmechanismus könne nur als Ganzes ausgelesen werden.
Der Hebelmechanismus tritt zwar bei den meisten Salbeiarten auf, ist aber nicht für eine erfolgreiche Pollenübertragung notwendig. Die Fülle alternativer Bestäubungsmechanismen, vor allem die Reduktion des Hebelmechanismus mit dem Übergang zur Vogelbestäubung, weist darauf hin, dass der Hebelmechanismus der Salbeiblüte nicht schlagartig "als Ganzes" ausgelesen wurde. Diese von den Evolutionskritikern vertretene Auffassung erscheint allenfalls plausibel, wenn man ein Beispiel wie den Wiesensalbei selektiv aus der Vielfalt herausgreift, ohne die strukturelle Diversität seiner Verwandten zu berücksichtigen.
Unabhängig vom Hebelmechanismus bei Salbeiarten kommt Intelligent Design nicht als wissenschaftliche Erklärung der Herkunft natürlicher Strukturen in Betracht. Zwar mag nichtreduzierbare Komplexität den Eindruck intelligenter Planung erwecken, doch fehlen empirische Methoden, um diese Hypothese zu testen. Lebewesen haben alle Eigenschaften, die sie für eine Evolution prädestinieren; nichts aus der Erfahrung spricht für schöpferische Akte. Vor diesem Hintergrund benötigt man eine mechanistische "Design"-Theorie, die erklären würde, wie die betreffenden Merkmalskomplexe ins Dasein gerufen wurden [28, S. 122]. Mangels eines solchen Erklärungsparadigmas ist "Design" keine wissenschaftliche Alternative zur Evolutionstheorie.
Um die Komplexität biologischer Systeme zu verstehen, müssen diese in ihrem funktionalen, entwicklungsmorphologischen und phylogenetischen Kontext gesehen werden. Die Gattung Salvia zeigt beispielhaft, dass sich von vorgegebenen Blüteneigenschaften (Prädispositionen) ausgehend ganz verschiedene Mechanismen zur Pollenübertragung entwickelt haben, darunter der Hebelmechanismus, der mehrfach parallel entstanden und wieder reduziert worden ist. Was manchem als "spielerische Komplexität" vorkommen mag, ist Ausdruck der natürlichen Vielfalt, die im Laufe der Evolution entsteht und das Potential zu vielfältiger Anpassung enthält.
Zusammenfassung
Evolutionskritiker verwenden den Hebelmechanismus in der Blüte des Wiesensalbeis als Beispiel, um die Existenz "nicht reduzierbarer" und "spielerisch komplexer" Strukturen zu belegen. Bezieht man allerdings die Entwicklung und Vielfalt der Salbeiblüten mit in die Betrachtung ein, zeigt sich, dass der Hebelmechanismus nicht schlagartig entstanden ist, sondern sich im Laufe von Millionen von Jahren durch natürliche Variation und Selektion entwickelt hat.

Summary: Evolution of "irreducibly complex systems": the lever mechanism of meadow sage
Critics of evolution use the lever mechanism in the fowers of meadow sage as an example to prove the existence of "irreducible" and "playfully complex" structures. However, considering the development and diversity of sage fowers, it becomes evident that the lever mechanism did not arise suddenly, but has evolved during millions of years due to natural variation and selection.
Schlagworte
Evolution, Hebelmechanismus, Intelligent Design, Salvia, Stamenkonstruktion
Literatur
[1] C. Funk et al. (2020). Biotechnology research viewed with caution globally, but most support gene editing for babies to treat disease. Pew Research Center 2020,1–49.
[2] D. Graf et al. (2011). Einstellung und Wissen von Lehramtsstudierenden zur Evolution – ein Vergleich zwischen Deutschland und der Türkei. In: Evolutionstheorie – Akzeptanz und Vermittlung im europäischen Vergleich (Hrsg. D. Graf), Springer, Heidelberg, 141–161.
[3] J. R. Downie et al. (2000). Evolution and religion: attitudes of Scottish first year biology and medical students to the teaching of evolutionary biology. J. Biol. Educ. 34, 139–146.
[4] W. Paley (1802). Natural theology: or, evidences of the existence and attributes of the deity. Faulder, London.
[5] D. Hume (1779). Dialogues concerning natural religion. London.
[6] C. Darwin (1859). On the origin of species by means of natural selection. Murray, London.
[7] R. Dawkins (1986). The blind watchmaker. Norton & Comp., New York.
[8] M. J. Behe (1996). Darwin’s Black Box. Free Press, New York.
[9] M. Mahner (2007). Intelligent Design und der teleologische Gottesbeweis. In: Kreationismus in Deutschland. Fakten und Analysen (Hrsg. U. Kutschera), Lit, Münster, 340–351.
[10] R. Junker et al. (2021). Schöpfung ohne Schöpfer? SCM Hänssler, Holzgerlingen.
[11] M. Widenmeyer et al. (2016). Der Kern des Design-Arguments in der Biologie und warum die Kritiker daran scheitern. http://www.wort-und-wissen.de/artikel/a22/a22.pdf.
[12] M. Neukamm (2022). Evolution und das Design-Argument in der Biologie. Ist Intelligent Design in der Natur belegbar? In: A. Losch & F. Vogelsang (Hg.) Gottes Schöpfung und menschliche Technik (S. 36–48). Theologie und Naturwissenschaft im Dialog III. wbg Academic, Darmstadt. https://www.ag-evolutionsbiologie.de/ html/2020/evolution-design-argument-biologie.html.
[13] R. Claßen-Bockhoff et al. (2004). Stamen development in Salvia L.: homology reinvestigated. Intern. J. Plant Sci. 165, 475–498.
[14] R. Claßen-Bockhoff (2024) Die Pflanze. Morphologie, Entwicklung und Evolution von Vielfalt. Kap. 11: Blumenstile und Bestäubungsmechanismen. Springer Spektrum, Heidelberg.
[15] J. Stöbbe et al. (2016). Training experiments with Bombus terrestris and Apis mellifera on artifcial 'Salvia' flowers. Flora 221, 92–99.
[16] B. T. Drew et al. (2012). Phylogenetics, biogeography, and staminal evolution in the tribe Mentheae (Lamiaceae). Amer. J. Bot. 99, 933–953.
[17] G. Guerin (2005). Floral biology of Hemigenia and Microcorys (Lamiaceae). Austr. J. Bot. 53, 147–162.
[18] P. Endress (2016). Development and evolution of extreme synorganization in angiosperm fowers and diversity: a comparison of Apocynaceae and Orchidaceae. Ann. Bot. 117, 749–767.
[19] F. Weberling (1981). Morphologie der Blüten und Blütenstände. Ullmer, Stuttgart.
[20] R. Claßen-Bockhoff (2017). Stamen construction, development and evolution in Salvia s. l. Nat. Vol. Essent. Oils 4, 28–48.
[21] Y. Ajani et al. (2022). Floral biology in the endemic Iranian Salvia majdae – implications for taxonomy, character evolution and conservation. Flora 287, 151986.
[22] R. Kriebel et al. (2023). Evolution of anther connective teeth in sages (Salvia, Lamiaceae) under bee and hummingbird pollination. Flora 298, 152199.
[23] P. Wester et al. (2007). Floral diversity and pollen transfer mechanism in bird-pollinated Salvia species. Ann. Bot. 100, 401–421.
[24] D. Ott et al. (2016). Salvia apiana – a carpenter bee flower? Flora 221, 82–91.
[25] H. W. Xiao et al. (2024). Mixed mating patterns in morphologically diverse bumblebee-pollinated Salvia species from China. Biol. J. Linn. Soc. 143(1), blad164.
[26] R. Kriebel et al. (2019). Tracking temporal shifts in area, biomes, and pollinators in the radiation of Salvia (sages) across continents: leveraging anchored hybrid enrichment and targeted sequence data. Amer. J. Bot. 106(4), 573–597.
[27] M. Will et al. (2017). Time to split Salvia s.l. (Lamiaceae) – new in-sights from Old World Salvia phylogeny. Mol. Phyl. Evol. 109, 33–58.
[28] M. Mahner (2018). Naturalismus. Die Metaphysik der Wissenschaft. Alibri, Aschaffenburg.


